من اللقاحات المركبة بتقنية mRNA إلى العلاجات الموجهة لأورام الأطفال: تسعى وكالة الأدوية الأوروبية إلى تحقيق توازن جديد بين الابتكار، والفائدة السريرية، والمسؤولية الاجتماعية.
بقلم إيهاب سلطان
HoyLunes – من مقرها الرئيسي في أمستردام، لا تقتصر مهمة وكالة الأدوية الأوروبية (EMA) على التحقق من صحة الجزيئات فحسب، بل تعيد تعريف الإطار التشغيلي للرعاية الصحية الأوروبية للعقد القادم. مع بداية عام 2026، تقف أوروبا على مفترق طرق، حيث تُجبر الكفاءة التكنولوجية – التي تمثلها تقنية mRNA – والطب الدقيق – الذي يتجسد في طب أورام الأطفال – على إعادة النظر في حجم الاستثمار الذي ترغب فيه، والشروط التي يجب أن تُبنى عليها، لدعم التقدم الطبي الحيوي.
عصر التطعيم المركب: فعالية جرعة واحدة
في فبراير 2026، أصدرت لجنة المنتجات الطبية للاستخدام البشري (CHMP) توصية إيجابية للقاح mCombriax، وهو أول لقاح مركب بتقنية mRNA ضد الإنفلونزا الموسمية وفيروس SARS-CoV-2، مُخصص لمن تزيد أعمارهم عن 50 عامًا. لا يُعد هذا ترخيصًا روتينيًا، بل يُشير إلى بداية تطبيع استخدام منصة mRNA خارج نطاق حالات الطوارئ الوبائية.
من خلال دمج وسيلتي حماية في قارورة واحدة، تُرسل وكالة الأدوية الأوروبية (EMA) إشارة استراتيجية مفادها أن سهولة الاستخدام السريري والكفاءة التشغيلية أصبحتا من أهم عوامل الصحة العامة.
الآلية المؤسسية الأوروبية
تجدر الإشارة إلى أن وكالة الأدوية الأوروبية لا “تُصادق” على الأدوية بالمعنى القانوني الدقيق. تُصدر لجنة المنتجات الطبية للاستخدام البشري (CHMP) رأيًا علميًا قائمًا على الجودة والسلامة والفعالية؛ أما القرار الرسمي فيعود إلى المفوضية الأوروبية، التي تمنح ترخيصًا ساريًا في جميع الدول الأعضاء. بعد ذلك، تتفاوض كل دولة على السعر وشروط السداد.
يفصل هذا النظام عمدًا بين التقييم العلمي واتخاذ القرارات الاقتصادية، مما يحمي كلًا من الدقة التنظيمية والاستدامة المالية.
التوقعات التنظيمية والأثر على الميزانية
من الناحية التقنية، تتوقع mCombriax توسع نطاق اللقاحات متعددة التكافؤ التكيفية. ومن المتوقع أن يتم، في السنوات القادمة، ترسيخ إطار عمل لتحديثات السلالات السريعة، يجمع بين نموذج الإنفلونزا التقليدي والسرعة التقنية لتقنية mRNA.
الأثر المحتمل على الميزانية:
انخفاض التكاليف اللوجستية: قد يؤدي استخدام نظامي إعطاء اللقاح إلى خفض نفقات تشغيل الحملات بنسبة تتراوح بين 15% و20% عن طريق تقليل الزيارات السريرية ومتطلبات سلسلة التبريد المكررة.
الاستدامة الاقتصادية الكلية: على الرغم من أن سعر الوحدة أعلى من اللقاحات التقليدية القائمة على البروتين، إلا أن انخفاض حالات دخول المستشفيات بسبب العدوى المصاحبة يمكن أن يعوض الاستثمار خلال دورة موسمية واحدة.
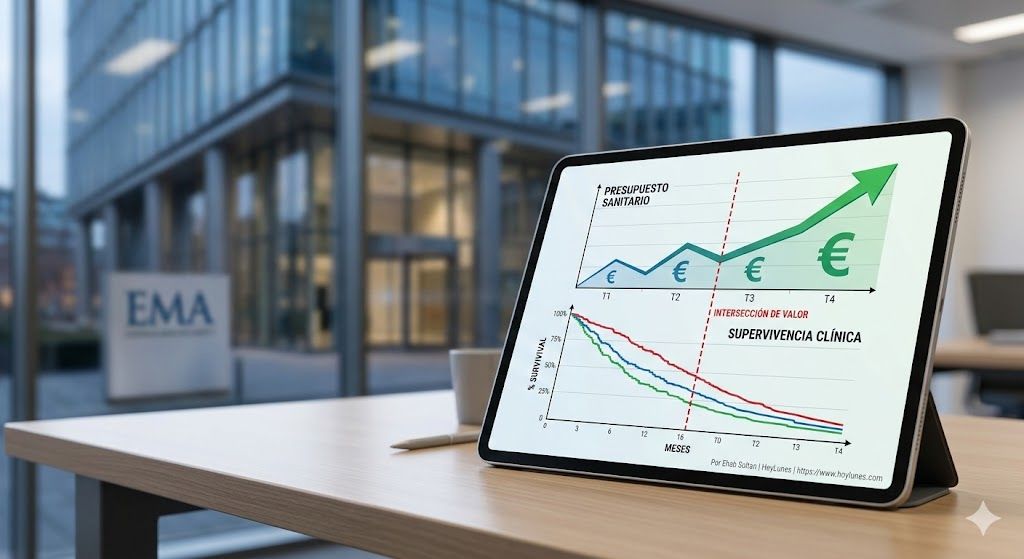
يمثل الإنفاق على الأدوية ما يقارب 15% إلى 20% من إجمالي الإنفاق على الرعاية الصحية في الاتحاد الأوروبي، مع نمو مستمر مدفوع بالعلاجات السرطانية والأدوية اليتيمة. في مجال الأورام، تجاوزت الزيادة التراكمية منذ عام 2020 نسبة 30% في العديد من الدول الأعضاء. إن الدمج المتزامن للقاحات المركبة والعلاجات الدقيقة يستلزم مراجعة نماذج التمويل في الأنظمة التي تواجه شيخوخة سكانية وضغوطًا هيكلية.
إذا كانت اللقاحات المركبة ترمز إلى كفاءة السكان، فإن طب أورام الأطفال يمثل الطرف الآخر من الطيف التنظيمي: علاجات شديدة التخصص تستهدف فئات صغيرة ولكنها ذات حالات سريرية عاجلة. فبينما يُحسّن التحصين الأنظمة، يُعيد الطب الدقيق تعريف القيمة الفردية لكل حياة.
أوجيمدا: عندما تصل الدقة إلى أشدّ المرضى ضعفًا
يُمثّل دواء أوجيمدا (توفورافينيب) المحور الثاني لهذا التحوّل، وهو مُخصّص لحالات مُحدّدة من أورام الدماغ منخفضة الدرجة لدى الأطفال (pLGG). بالنسبة للمرضى الذين لا يستجيبون للجراحة أو العلاج الكيميائي، كانت البدائل العلاجية التقليدية محدودة.
بمعدلات استجابة تقارب 71%، لا يُوقف توفورافينيب نمو الورم فحسب، بل يُقلّل أيضًا من التعرّض للسمية الجهازية المُصاحبة للأنظمة العلاجية التقليدية القائمة على كاربوبلاتين وفينكريستين، والتي تشمل سمية عصبية تراكمية، وكبت نخاع العظم، وإقامة مُطوّلة في المستشفى.
علاوة على ذلك، لطالما كان البقاء على قيد الحياة دون تفاقم المرض لدى المرضى المُقاومين للعلاج محدودًا، مع تأثيرات كبيرة على الوظائف الإدراكية والغدد الصماء. في هذا السياق، لا يُمثّل المُثبّط الانتقائي ذو الخصائص الجزيئية المُستهدفة تقدّمًا علاجيًا فحسب، بل يُمثّل نقلة نوعية في تقييم المخاطر والفوائد.
مع ذلك، يُعيد ترخيص هذا الدواء فتح النقاش حول الطب المتخصص واستدامة الأدوية اليتيمة باهظة الثمن.
الأدلة الواقعية ونماذج الدفع
تعمل وكالة الأدوية الأوروبية على تعزيز آليات **الأدلة الواقعية** لمراقبة هذه العلاجات بعد طرحها في الأسواق. يتمثل التحدي الذي يواجه الأنظمة الوطنية – مثل نظام SNS في إسبانيا، ووكالة AIFA في إيطاليا، وهيئة HAS/ANSM في فرنسا – في ترسيخ نماذج الدفع مقابل الأداء: أي التمويل المشروط بتحقيق فائدة سريرية مستدامة.
ينقل هذا النهج جزئيًا المخاطر المالية إلى قطاع الصناعة، ويتطلب بنى تحتية قوية وشفافة للبيانات.
الوصول، والأدوية الحيوية المماثلة، والتوازن في الميزانية
في اجتماعها الأخير، أوصت لجنة المنتجات الطبية للاستخدام البشري (CHMP) باثني عشر دواءً جديدًا، ووسعت نطاق ستة مؤشرات إضافية. بالتوازي مع ذلك، تكثفت الجهود المبذولة لتطوير الأدوية الحيوية المماثلة والأدوية البيولوجية من الجيل الثاني، باعتبارها أدوات رئيسية لكبح التكاليف وتوسيع نطاق الوصول.
تفقد الابتكارات شرعيتها إذا أدت إلى اتساع فجوات عدم المساواة بين الدول الأعضاء. في عام 2026، يُقاس الدور التنظيمي لوكالة الأدوية الأوروبية (EMA) بجودة آرائها العلمية بقدر ما يُقاس بأثرها التوزيعي.
أوروبا مقابل إدارة الغذاء والدواء الأمريكية والمنافسة العالمية
بينما وسّعت إدارة الغذاء والدواء الأمريكية آليات الموافقة السريعة، تحافظ وكالة الأدوية الأوروبية على توجه مقارن أكثر حذرًا، يركز على القيمة العلاجية المضافة.
يُعدّ هذا الاختلاف ثقافيًا أيضًا. فالنموذج الأمريكي يُعطي الأولوية لديناميكية السوق، بينما يُشدد النموذج الأوروبي على المتانة النسبية والتقييم التدريجي للفائدة السريرية. سيؤثر هذا التباين على القدرة التنافسية للصناعات الدوائية الحيوية خلال العقد القادم، لا سيما في ظل تزايد الاستثمارات الصينية في التكنولوجيا الحيوية والتجارب اللامركزية.
تواجه أوروبا معضلة استراتيجية: تجنب أن تصبح مجرد جهة تنظيمية لتقييم الابتكارات الخارجية، وترسيخ مكانتها كمحركها الخاص للبحوث التطبيقية.
توقعات 2026-2030
لامركزية التجارب السريرية: زيادة تكامل التطبيب عن بُعد والأجهزة الرقمية لتوسيع نطاق المشاركة الجغرافية.
الذكاء الاصطناعي في اليقظة الدوائية: أنظمة الكشف المبكر عن الآثار الجانبية قادرة على تقليص مدة الاستجابة من شهور إلى أيام.
مع ذلك، يتطلب التسارع التنظيمي الحذر. فالاعتماد المتزايد على البيانات المؤقتة، والدراسات أحادية المجموعة، والأدلة الواقعية، يستلزم مراجعات دورية صارمة، وقدرة حقيقية على سحب المنتجات في حال عدم تأكيد الفوائد. وتعتمد ثقة الجمهور على السرعة لا على الدقة.
العقد الاجتماعي الجديد للرعاية الصحية
من الناحية الهيكلية، تعمل وكالة الأدوية الأوروبية كوسيط لعقد اجتماعي متجدد في مجال الرعاية الصحية. يقبل المواطنون تمويل الابتكارات عالية التكلفة على أساس الوصول العادل والأدلة القوية. وفي المقابل، يحصل القطاع على استقرار تنظيمي وسوق موحدة.
عندما يختل هذا التوازن – بسبب الأسعار غير المتناسبة أو الأدلة غير الكافية – تتآكل شرعية النظام.
موازنة بين العلم والضمير
تُظهر القرارات التنظيمية لعام ٢٠٢٦ أن الطب المعاصر يُمثل عملية موازنة مستمرة بين الابتكار والإنصاف والاستدامة. لن يعتمد نجاح أوروبا على عدد الأدوية المُرخصة فحسب، بل على قدرتها على دمج الكفاءة التكنولوجية والدقة العلاجية والاستقرار المالي للأنظمة العامة في آنٍ واحد.
لم يعد السؤال الاستراتيجي هو ما إذا كانت أوروبا قادرة على الابتكار، بل ما إذا كانت قادرة على الحفاظ على هذا الابتكار دون المساس بنموذجها للتضامن في الرعاية الصحية. في خضم هذا التوتر، سيُرسم الفصل التالي من تاريخ الطب الأوروبي.
ستعتمد شرعية الطب الأوروبي في المستقبل ليس فقط على قدرته على التطور، بل أيضاً على قدرته على اتخاذ قرارات حكيمة بشأن أيّ التطورات تستحق التمويل الجماعي.
المصادر الموصى بها
البيانات الرسمية للجنة المنتجات الطبية للاستخدام البشري (CHMP) ووكالة الأدوية الأوروبية (EMA)
تقارير التقييم العام الأوروبي (EPAR)
المركز الأوروبي للوقاية من الأمراض ومكافحتها (ECDC) (بيانات وبائية وبيانات التطعيم)
منظمة التعاون الاقتصادي والتنمية – نظرة عامة على الصحة
بيانات الإنفاق على الأدوية من IQVIA والاتحاد الأوروبي للصناعات الدوائية (EFPIA)
#الابتكار_التنظيمي_2026 #التكنولوجيا_الحيوية #وكالة_الأدوية_الأوروبية #HoyLunes #إيهاب_سلطان #وكالة_الأدوية_الأوروبية #الصحة_العامة #الطب_الدقيق